카타라 : 물을 이렇게 밀었다가 당겨봐. 비결은 팔목을 잘 쓰는거야.
아앙 : 이렇게? (워터밴딩으로 냇물을 조종하는 아앙)
- 애니 <아바타 : 아앙의 전설> 중에서 -

지표와 생물의 대부분을 차지하는 물
인류를 비롯한 모든 생물에게 있어서 가장 중요한 물질이며, 생체의 주요한 성분이다. 인체는 약 70%, 어류는 약 80%, 그 밖에 물 속의 미생물은 약 95%가 물로 구성되어 있다. ... 물은 지표면의 71% 정도를 덮고 있으며 지구상에 존재하는 전체 물의 97.5%는 바닷물이다. - 위키백과 -
다른 행성들보다도 물이 풍부한 지구. 태양과의 거리도 적당하고 평온하게 다이나믹한 환경조건이 만들어진 이곳에 생명이 탄생하고 자리잡다. 우리는 이곳에 태어난 생명 중 하나이면서 아직까지도 우리 지구 생물외의 독자적으로 탄생한 생명체를 찾지 못했다. 풍부한 지표의 물처럼 우리와 다른 생명들의 체내에는 물로 가득차 있으며 우리는 이 물에 의존하는 수준을 넘어서 사실상 물이 우리를 만든다고 해도 과언이 아닐 정도이다. 오늘은 이 물에 대해 알아보고자 한다.
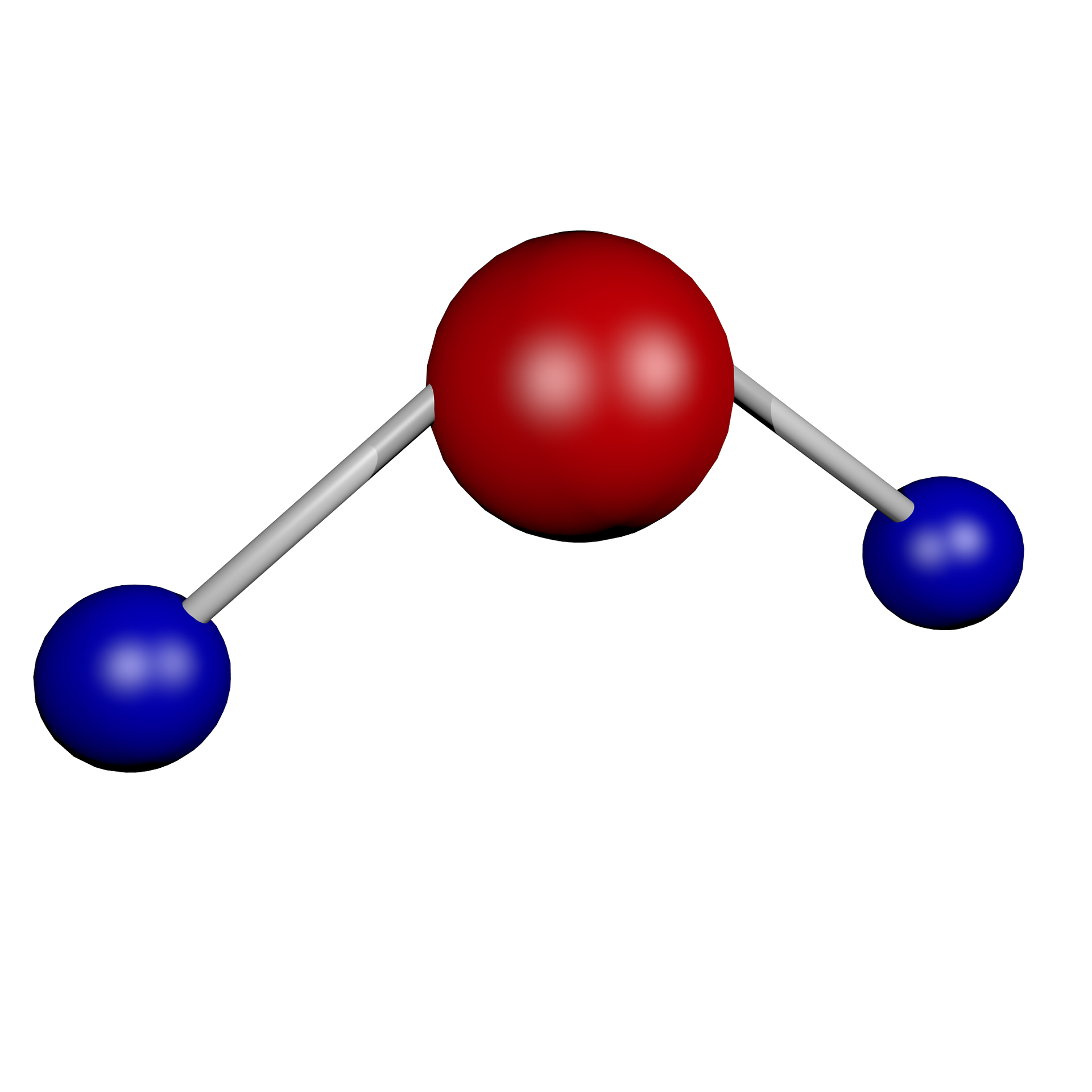
물분자의 구조
원자번호 8번인 산소는 양성자 8개인 원소이고 양성자 1개인 수소 2개와 만나 H2O를 구성한다. 분자량은 18.01528g/mol로 물분자 1mol개 (6.02214076 x 10^23개) 모여있다면 18g정도가 된다. 그림에서도 알 수 있듯이 특이하게도 물분자의 모습은 굽어진 꺾쇠 모양으로 표현되어있다. (내용출처 : 위키백과) 이는 실제로 물분자가 이렇게 굽어진채 산소와 수소사이 결합을 이루고 있기 때문이다. 산소는 전자 껍질에 2개의 전자가 더 채워진 상태가 더 안정한데 수소원자 2개가 가진 전자를 하나씩 공유하여 공유결합을 이룬다. 이때 산소에 있던 전자 중 결합하지 않는 나머지 4개의 전자는 2개씩 비공유 전자쌍을 이루어 총 4개의 전자쌍들이 서로 반발하게 된다. 산소와 수소의 결합전자쌍(BP, bond pair)보다 비공유전자쌍(LP, lone pair)들이 중심원자에의해 더 끌어당겨지기에 더 강하게 반발하는데 이 미묘한 차이가 힘의 균형을 이루어 수소-산소-수소의 결합각도는 약 104.5°를 유지한다. (내용출처 : CHEMTAK 화학 심층면접/탁주환/도서출판 좋은땅) 치우쳐진 비공유전자쌍과 수소원자들 때문에 물분자는 전기적으로 극성을 띤 세상에서 가장 작다고 할 수준의 자석이 된다. 여기서 물의 대부분의 성질이 발생한다.
물분자의 구조에 대해 가볍고 알기쉽게 설명되어있는 페이지도 있다.
물정보에 대한 모든것 - MyWater
물 분자는 어떤 모양일까? 물 분자는 어떻게 생겼을까? 나뭇잎 끝에 달린 아침이슬처럼 동그랗게 생겼을까? 아니면 각설탕처럼 네모일까? 산소를 가운데 놓고 두 개의 수소 원자와 두 쌍의 비결
m.water.or.kr:443
물리적 성질
모두가 알듯이 물은 0°C에서 얼고 100°C에서 끓는다. 사실 섭씨온도의 기준 자체가 물이기 때문에 그러하다. 켈빈과 화씨모두 비교하자면 물의 녹는점은 273.15 K, 32°F, 0.00°C 이고 끓는점은 373.14 K, 211.982°F, 99.99°C 이다. 밀도는 4°C 기준 1 g/cm^3 이고 온도가 높아질수록 낮아진다. (내용출처 : 위키백과) 물의 중요한 특징중 하나는 4°C 부근에서 밀도가 최대가 되고 이보다 낮은 온도에서 얼음이 될때까지 밀도가 조금씩 감소한다는 것이다. 액체상태의 물은 열에너지를 잃을수록 서로 부딪히는 속력이 감소하고 분자들간의 거리가 가까워 진다. 이렇게 4°C가 될때까지 거리가 좁혀지다가 어떤 분자들은 서로 어느정도 붙어버린 고체 물, 즉 얼음구조를 일부 형성하게 되는데 얼음의 구조는 전기적양성인 수소와 전기적음성인 산소가 수소결합이 강하게 영향을 발휘할 정도로 가까워지기때문에 그 각도가 묘하게 잘 맞춰져서 육각형의 모습을 보인다. 물이 얼음이 되면서 그 육각형의 빈공간으로 인해 부피가 약 10%가 증가해버리고 일반적인 다른 분자들과는 다르게 분자끼리 더 가까워진 고체의 물은 액체보다 부피가 더 크다.


화학적 성질
물의 화학적 성질은 수소결합(hydrogen bond)으로 거의 대부분 설명이 된다.
전기음성도(electronegativity)가 강한 질소(N), 산소(O), 플루오린(F) 등의 원자에 수소(H) 원자가 공유결합으로 결합하면 전기음성도가 강한 원자는 부분적인 음(-)전하를 띄고 수소 원자는 부분적인 양(+)전하를 띠게 된다. 이러한 수소 원자에 전기음성도가 강한 원자가 서로 이웃하게 되면 이 두 원자 사이에 정전기적 인력이 생기는데 이것을 수소결합(hydrogen bond)이라 한다. - 네이버 지식백과 -
사실 수소결합은 물에서만 나타나는 것은 아니고 전기음성도가 강한 원자에 붙은 바깥 수소가 있을경우 가까운 다른분자에 전기음성도가 강한 원자가 있다면 생길 수 있다. 하지만 각각 그 결합력은 결합되는 원자의 종류와 특성에 따라 달라지고 물의 경우 결합력은 3.00 kcal/mol 정도로 보인다. (내용출처 : Theoretical Study on the Hydrogen-Bonding Effect of H2On-H2Om (n=1-4, m=1-4) Dimers/ Hui-Seong et al. / 2015 / Journal of the Korean Chemical Society) 엄청 강하지도 또 결코 약하지도 않은 이 결합력이 분자들이 멀어지는데에 더 많은 에너지를 필요로 하게 하고 이때문에 발생한 비열로 인해 언뜻 비슷해보이는 다른 분자들이 기체로 존재할 때 물은 고체나 액체로 존재한다(암모니아 녹는점 -77.73°C, 에탄올 녹는점 -114.14°C, 이산화탄소 녹는점 -56.6°C, 메탄 녹는점 -182.5°C). 소주마실때 잘 알 수 있는 표면장력과 모세관 현상도 이 수소결합으로 인해 발생한다.
물은 보통 금속류를 녹여 염기를 만들고 비금속류를 녹여 산을 만든다. 산과 염기의 기준은 양이온으로 하전된 수소 이온과 음이온으로 하전된 수산화이온이며, 수소이온이 많으면 산성이고 수산화이온이 많으면 염기성이며, 두 이온의 값이 0에 가까우면 중성이 된다. ... 물은 산소와 함께 금속을 잘 부식시키는 성질이 있다. 철의 경우 반응성이 크나 직접적으로는 산소와 잘 반응하지 않으며 아주 천천히 산화철을 생성한다. - 위키백과 -
궁금한점
- 비공유전자는 왜 굳이 쌍으로 존재하려고 할까?
- 물분자의 각도가 어떤 힘에 의해 더 기울어지는 경우는 없을까? 있다면 어떤힘이 얼마나 필요할까?
- 이성질체 원자가 섞여있다면 성질이 어떻게 달라질까?
'자연과학 > 화학' 카테고리의 다른 글
| 하나여도 좋지만 둘이면 항상 함께 한다, 비공유 전자쌍 (0) | 2022.12.18 |
|---|---|
| 산소 마스크 없는 배양캡슐액의 정체, 퍼플루오린화탄소 (2) | 2022.11.26 |
| pH(수소 이온 농도 지수) (0) | 2022.07.27 |
| 그대 만을 위한 오메가-3 (0) | 2022.07.15 |